近期,复旦大学药学院王建新教授课题组和庞志清副教授课题组合作开发了一种新型的仿生红细胞膜融合脂质体,并进行了细菌毒素清除和耐药细菌感染治疗相关研究。3月11日,相关成果以《仿生红细胞膜融合脂质体用于成孔毒素清除》(Erythroliposomes: Integrated Hybrid Nanovesicles Composed of Erythrocyte Membranes and Artificial Lipid Membranes for Pore-Forming Toxin Clearance)为题,在线发表于《美国化学学会-纳米》(ACS NANO)。
目前,细菌感染仍然是世界范围内的一类高发病率和高致死率的疾病,而耐药细菌尤其是“超级细菌”的出现给细菌感染治疗带来了更大挑战。目前全球新型抗生素的研发进展停步不前,新型抗生素匮乏,亟需设计和开发新型的给药策略以改善耐药细菌感染的治疗效果。
成孔毒素是细菌感染的主要毒力因子,在细菌感染过程中协助病原菌的生长、侵袭和定殖。针对成孔毒素的抗毒力因子治疗策略可通过非直接杀灭病原菌避免细菌产生耐药,是耐药细菌感染治疗的重要方向。近年来,随着纳米技术的发展,采用纳米药物抗毒力因子治疗耐药细菌感染的研究方向受到越来越多科学家的关注。
然而,细菌在感染过程中不断产生成孔毒素,对纳米药物吸附毒素能力提出了极大的挑战。针对现有纳米药物体内清除毒素能力不足的问题,王建新课题组和庞志清课题组的研究以α-溶血素(Hlα)为代表性成孔毒素,根据成孔毒素与细胞膜的相互作用原理,基于仿生策略,设计了一种新型的仿生红细胞膜融合脂质体用于毒素的吸附与清除(图1)。该仿生脂质体结合天然红细胞膜和人工脂质膜的优点,既充分利用红细胞膜成分协助成孔毒素的膜插入作用,又利用人工脂质膜的空间优势,极大地提高了红细胞膜的毒素清除能力(139倍),可实现高剂量成孔毒素的有效吸附,显著降低成孔毒素对模型小鼠的侵害作用。由于生物膜与人工脂质膜较易融合,该仿生脂质体制备方法简单,既能有效保持膜蛋白的活性,又利于实现工业化。因此,该研究为耐药细菌感染的治疗提供了新的思路。
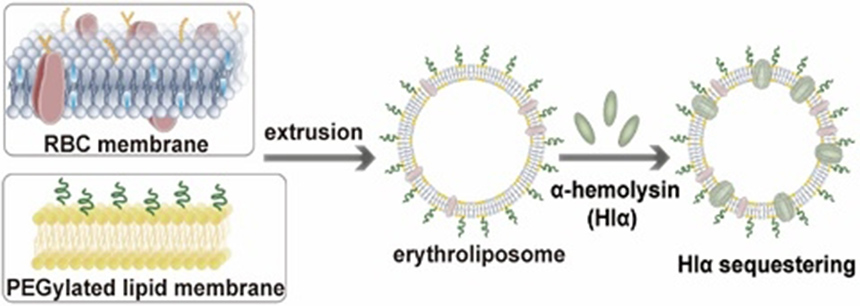
图1
复旦大学药学院博士研究生何雨薇和李瑞翔为论文的共同第一作者,王建新和庞志清为论文的共同通讯作者。该研究获得国家自然科学基金委和上海市科委重点项目的支持。